يرتبط ML بالتشخيص لدى المرضى الذين يعانون من نظام التشغيل
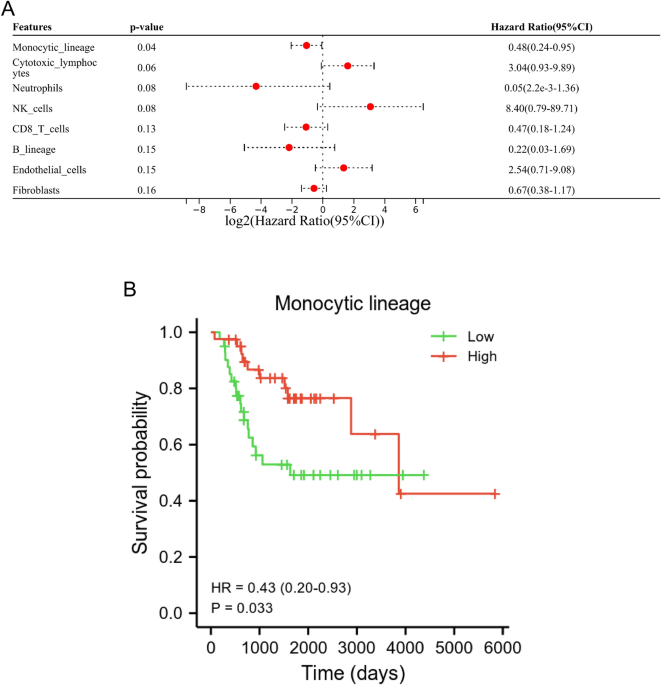
في دراستنا، تم إجراء خوارزمية مضادة لـ MCP وتحليل انحدار كوكس أحادي المتغير وأحادي المتغير لتحديد الخلايا المناعية المرتبطة بالبقاء على قيد الحياة. وأظهرت نتائج تحليل انحدار كوكس أحادي المتغير أن ML كان عبارة عن خلية مناعية مرتبطة بالبقاء على قيد الحياة لدى مرضى OS (الشكل 1A). بالإضافة إلى ذلك، أشار تحليل كابلان ماير إلى أن المستوى المنخفض من ML كان مرتبطًا بسوء التشخيص لدى مرضى OS (ع = 0.033، الشكل 1ب).
يرتبط ML بسوء التشخيص لدى المرضى الذين يعانون من نظام التشغيل. (أتحليل كوكس أحادي المتغير لستة خلايا مناعية وخليتين انسجتين بناءً على قاعدة بيانات TARGET. (ب) أظهر تحليل كابلان ماير أن مستوى ML كان مرتبطًا بشكل كبير بتشخيص المرضى.
تحليل DEGs ومسارات الإشارات المحتملة بين المجموعتين الفرعيتين
تم تحديد ما مجموعه 435 DEGs بعد تحليل DEGs (الشكل 2A، B). بالمقارنة مع LML، تم تنظيم 101 جينًا وتم تنظيم 334 جينًا في مجموعة HML. أثناء العمليات البيولوجية (BP)، تشارك هذه DEGs في تنظيم المكونات الخلوية مثل تنشيط الخلايا الليمفاوية، وتنشيط الخلايا التائية، والتنظيم الإيجابي لتنشيط الخلايا، وتنشيط الخلايا التائية، والتصاق خلايا الكريات البيض، وما إلى ذلك. (CC)، وتشارك DEGs في الجانب الخارجي من غشاء البلازما، والغشاء الحبيبي الإفرازي، والحبيبات الغنية بالفيكولين 1، والمشبك المناعي، ومجمع أوكسيديز NADPH، وما إلى ذلك. خلال فترة الوظائف الجزيئية (MF)، تم إثراء DEGs بشكل كبير في الكربوهيدرات. الربط، ربط مستقبلات السيتوكين، ربط السيتوكين، نشاط مستقبل السيتوكين، نشاط مستقبل السيتوكين CC، إلخ. خلال KEGG، تم إثراء DEGs بشكل رئيسي في نسب الخلايا المكونة للدم، وتمايز الخلايا العظمية، ومستقبلات مستقبلات السيتوكينات السيتوكينية التي تشير إلى B. المسار، وما إلى ذلك (الشكل 3).
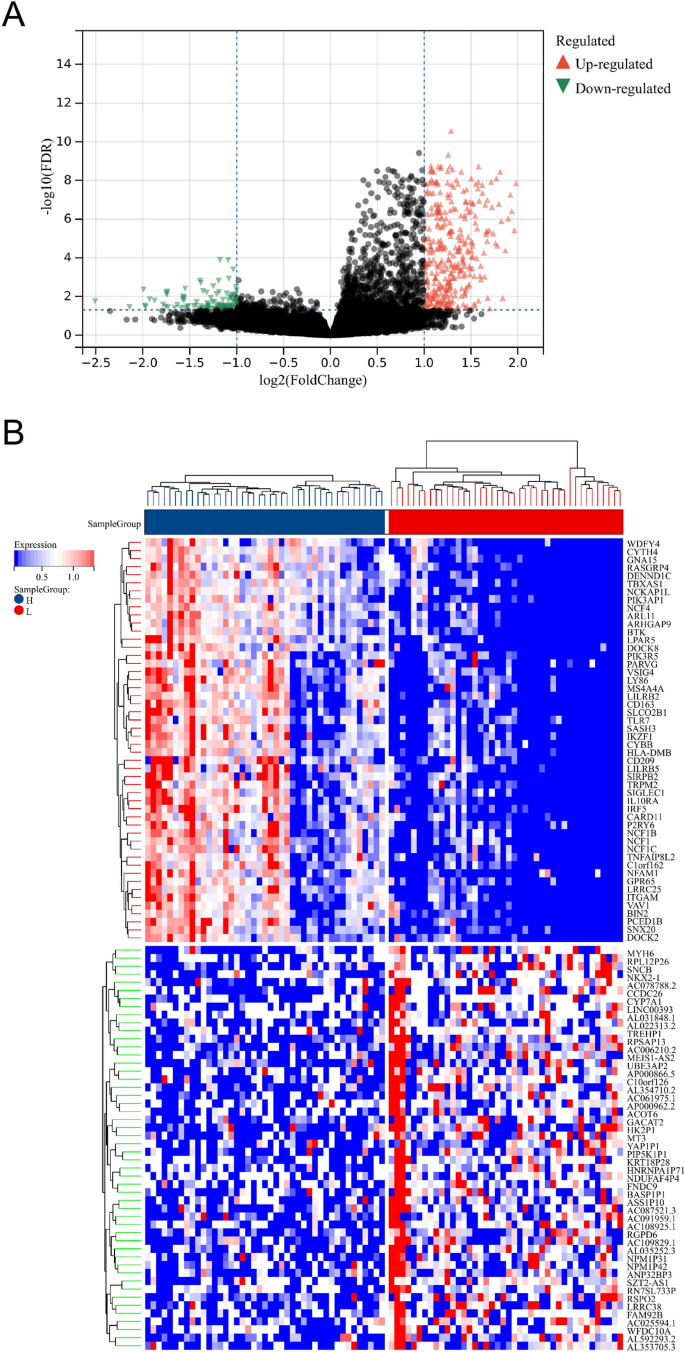
تحديد DEGs بين مجموعات LML وHML الفرعية. (أ) مؤامرة البركان تصور DEGs بين مجموعات LML و HML الفرعية. تشير النقاط الخضراء إلى الجينات الخاضعة للتنظيم السفلي، في حين تشير النقاط الحمراء إلى الجينات الخاضعة للتنظيم. (ب) مؤامرة خريطة الحرارة التي تصور أعلى 50 درجة بين مجموعات فرعية LML وHML.
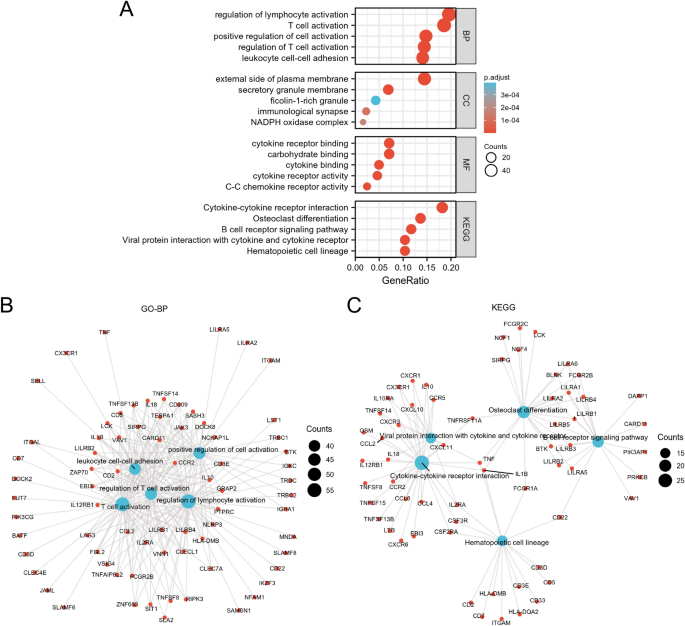
تحليل إثراء DEGs. (أ) تصور المؤامرات الفقاعية نتائج GO وKEGG. رسم تخطيطي للشبكة يصور مصطلحات GO-BP المتعلقة بالمناعة والالتهابات (ب) ومسارات KEGG (ج) تمثل العقد الزرقاء مصطلحات GO-BP أو مسارات KEGG، وتمثل العقد الحمراء الجينات المشاركة في المسارات.
تسلل الخلايا المناعية
قمنا بتحليل الحالة المناعية بين مجموعات فرعية LML وHML لفهم البيئة المكروية المناعية في نظام التشغيل. كما هو مبين في الشكل 4A، بالمقارنة مع مجموعة HML، تم تخفيض النتيجة اللحمية والنتيجة المناعية ودرجة التقدير في مجموعة LML (ص<0.01)، تم زيادة نقاء الورم بشكل ملحوظ في مجموعة LML (ص<0.01). بالمقارنة مع مجموعة HML، انخفضت مستويات الخلايا البطانية والخلايا الجذعية النخاعية والنسب أحادية الخلية والنسب B والخلايا التائية وخلايا CD8 T بشكل ملحوظ في مجموعة CML (ص< 0.05) (الشكل 4B).
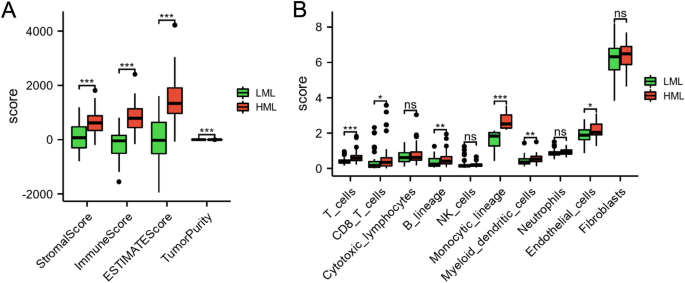
تضاريس مستويات تسلل الخلايا المناعية في مجموعتين فرعيتين. (أ) مقارنة النتيجة اللحمية، والنتيجة المناعية، والنتيجة التقديرية، ونقاء الورم بين المجموعات الفرعية LML وHML. (ب) مقارنات لمعدلات تسلل الخلايا المناعية بين مجموعات LML وHML الفرعية. *ص< 0.05، **ص<0.01، و ***ص<0.001.
بناء وتقييم نموذج المخاطر التنبؤية
بعد تحليل انحدار كوكس أحادي المتغير، قمنا بفحص 122 جينًا مرتبطًا بالبقاء على قيد الحياة (الجدول S1). بعد ذلك، حدد تحليل انحدار كوكس LASSO ثمانية جينات (CCDC26، TERT، GJA5، KRT18P28، LILRA6، PDE1B، CD180 وIL2RA) لتحليل انحدار كوكس متعدد المتغيرات (الشكل 5A، B). وأخيراً، تم فحص ثلاثة جينات مهمة مرتبطة بالبقاء بشكل عام (TERT، IL2RA وCCDC26) واستخدمت لإنشاء نموذج تنبؤي (الشكل 5C).
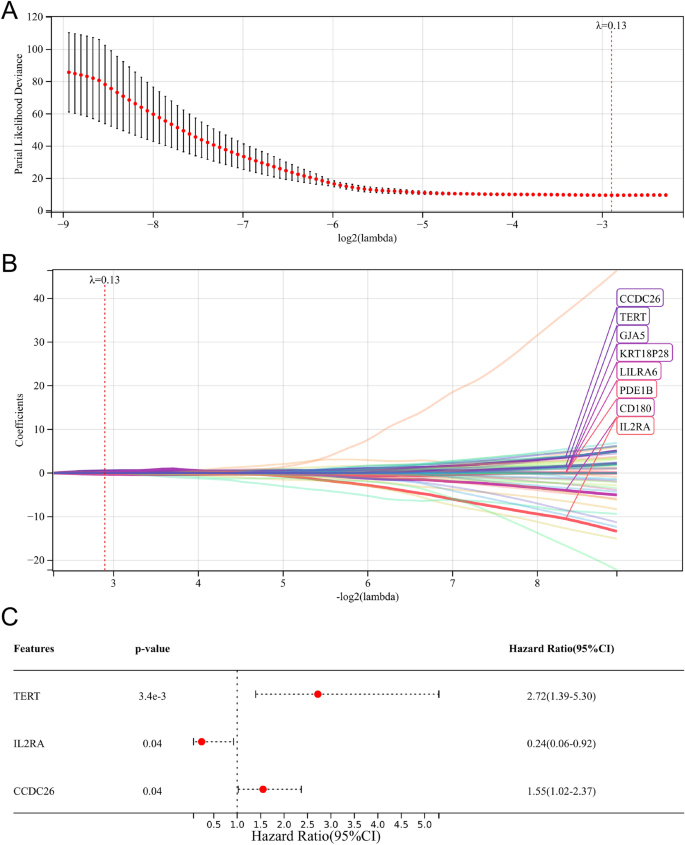
إنشاء نموذج تنبؤي مرتبط بتعلم الآلة. (أ, ب) تحليل الانحدار لاسو. (ج) تحليل انحدار كوكس متعدد المتغيرات.
في مجموعة بيانات TARGET، انخفض مستوى التعبير عن TERT وCCDC26 في المجموعة منخفضة المخاطر، في حين تم تنظيم التعبير عن IL2RA في المجموعة منخفضة المخاطر. أيضا، كان لدى المجموعة المعرضة للخطر معدل البقاء على قيد الحياة أقل (الشكل 6A). أظهر مرضى OS في المجموعة منخفضة الخطورة بقاء إجماليًا أطول من أولئك الموجودين في المجموعة عالية الخطورة (الشكل 6 ب، ص<0.001). كانت المساحة تحت المنحنى لهذا النموذج التنبؤي 0.8 في سنة واحدة، و0.87 في 3 سنوات، و0.85 في 5 سنوات (الشكل 6C)، مما يشير إلى أن هذه النتيجة كان لها أداء تشخيصي جيد لمرضى نظام التشغيل. استخدمنا مجموعة البيانات GSE21257 للتحقق من صحة الميزات التشخيصية والتنبؤية لنموذج المخاطر. كما هو مبين في الشكل 7A، تم تنظيم مستوى التعبير عن TERT وCCDC26 في المجموعة منخفضة المخاطر، بينما تم تنظيم التعبير عن IL2RA في المجموعة منخفضة المخاطر. كما نجت نسبة أقل في المجموعة المعرضة للخطر. أظهر مرضى OS في المجموعة منخفضة الخطورة بقاءًا إجماليًا أفضل من أولئك الموجودين في المجموعة عالية الخطورة (ص= 0.025) (الشكل 7B). وكانت AUC لهذا النموذج التنبؤي 0.84 في سنة واحدة، و0.67 في 3 سنوات، و0.68 في 5 سنوات (الشكل 7C). تتوافق هذه النتائج مع تلك الموجودة في مجموعة بيانات TARGET.
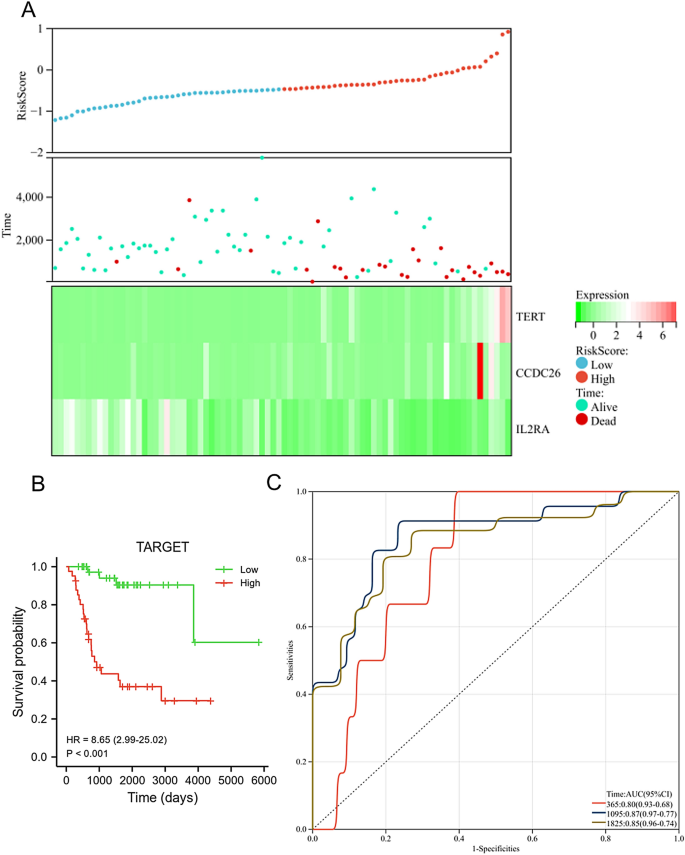
تقييم النموذج التنبؤي في قاعدة بيانات TARGET. (أ) مستوى التعبير عن TERT وCCDC26 وIL2RA (أسفل)، وحالة البقاء (الأوسط)، وتوزيع درجات المخاطر بين المجموعات المنخفضة والعالية المخاطر (أعلى). (ب) أظهر تحليل البقاء على قيد الحياة وجود فرق بين المجموعات المنخفضة والعالية المخاطر. (ج) تحليل منحنى ROC المعتمد على الوقت للنموذج التنبئي.
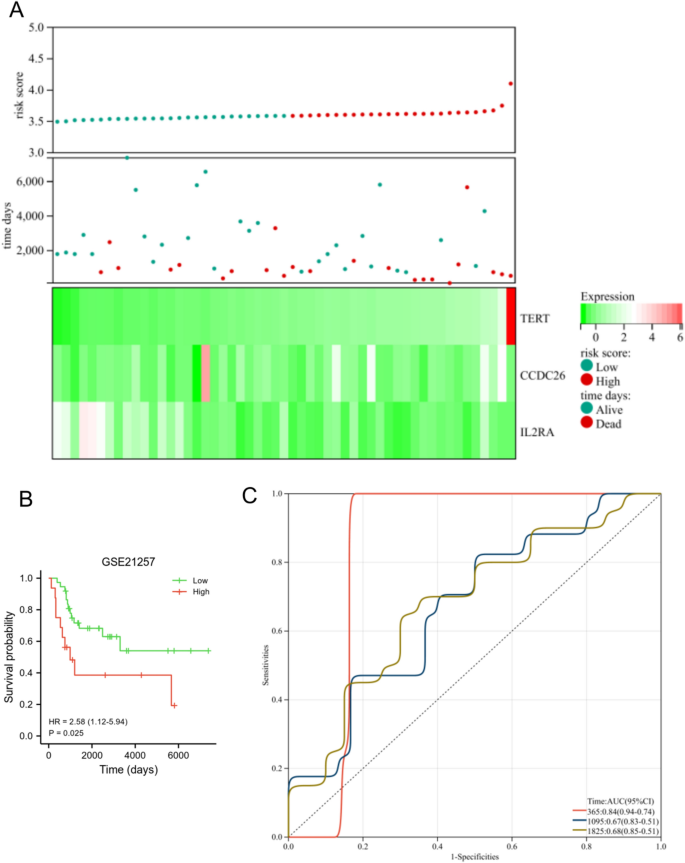
التحقق من صحة النموذج التنبؤي في مجموعة البيانات GSE21257. (أ) مستوى التعبير عن TERT وCCDC26 وIL2RA (أسفل)، وحالة البقاء (الأوسط)، وتوزيع درجات المخاطر بين المجموعات المنخفضة والعالية المخاطر (أعلى). (ب) أظهر تحليل البقاء على قيد الحياة وجود فرق بين المجموعات المنخفضة والعالية المخاطر. (ج) تحليل منحنى ROC المعتمد على الوقت للنموذج التنبئي.
وبالإضافة إلى ذلك، تم إنشاء مخطط بياني للمساعدة بشكل أكبر في التنبؤ بتشخيص مرضى نظام التشغيل (الشكل 8A). كانت نتائج التنبؤ للرسم البياني متسقة للغاية مع ملاحظة مرضى نظام التشغيل بناءً على منحنى معايرة الرسم البياني (الشكل 8 ب).
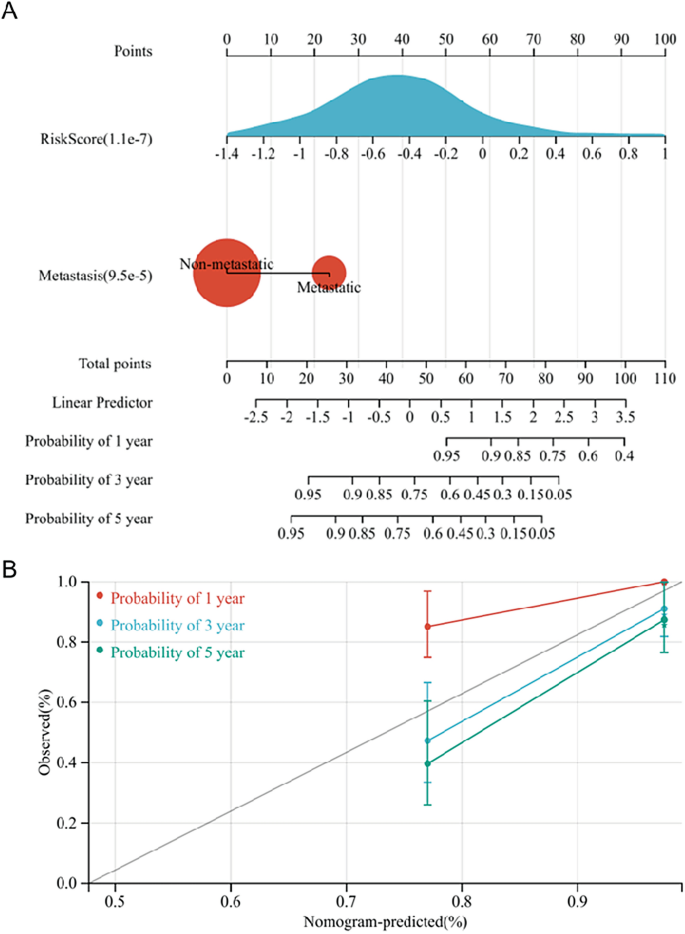
إنشاء مخطط بياني. (أ) استخدم ورم خبيث ودرجة المخاطر لإنشاء مخطط بياني. (ب) منحنى معايرة الرسم البياني.
تحليل الارتباط للجينات النذير
باستخدام قاعدة بيانات GeneMANIA، نجحنا في بناء شبكة تفاعل بروتينية لجينات التوقيع (TERT وIL2RA). من خلال هذا التحليل، اكتشفنا ما مجموعه 20 جينًا يشارك في التفاعلات مع جينات التوقيع (الشكل 9A). تم إجراء تحليل التخصيب الوظيفي على هذه الجينات الـ 22. أظهرت النتائج التي تم الحصول عليها من تحليل التخصيب أن هذه الجينات كانت مرتبطة بشكل أساسي بتنظيم التيلومير، وصيانة التيلومير، والعدوى بفيروس سرطان الدم في الخلايا التائية البشرية 1، وتمايز الخلايا Th1 وTh2 (الشكل 9B).
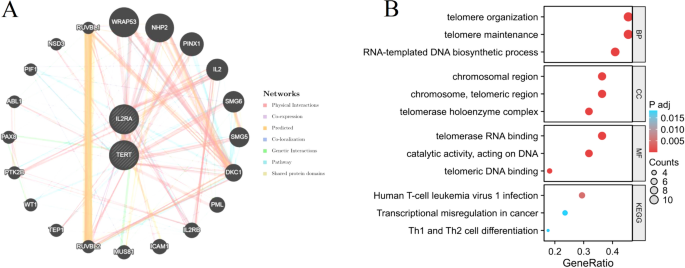
تحليل الارتباط للجينات التوقيع. (أ) شبكة التعبير المشترك لجينات التوقيع. (ب) تحليل التخصيب الوظيفي للجينات المعبر عنها بواسطة GO و KEGG.
العلاقة بين الجينات المرتبطة بنموذج المخاطر والبيئة الدقيقة للورم (TME).
باستخدام قاعدة بيانات TISCH، قمنا بتحليل مستويات التعبير عن جينات TERT وIL2RA في الخلايا المرتبطة بالبيئة الدقيقة للورم داخل نظام التشغيل. أظهرت النتائج التي توصلنا إليها أن IL2RA أظهر مستويات عالية من التسلل في خلايا CDC1، وحيدات الخلية، وM2 (الشكل 10).
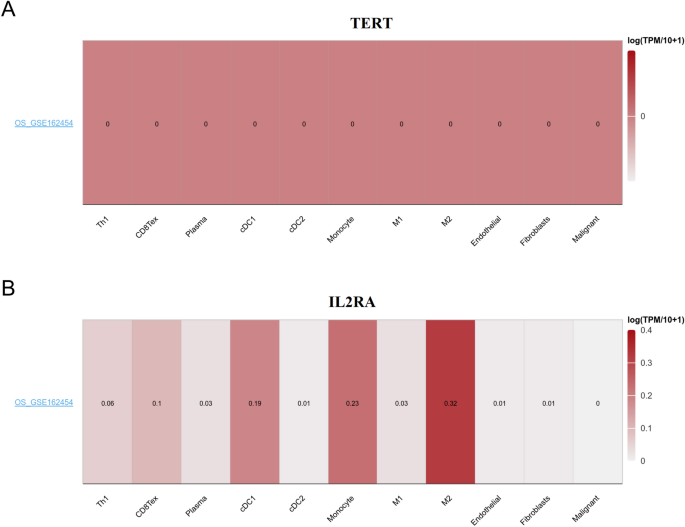
تم التعبير عن الجينات المرتبطة بأنماط الخطر في الخلايا ذات الصلة بالبيئة الدقيقة للورم. مستويات التعبير عن TERT (أ) وIL2RA (ب) تم تصور الخلايا المرتبطة بالبيئة الدقيقة في نظام التشغيل باستخدام خريطة حرارية من مجموعة بيانات GSE162454.
النموذج النذير لديه القدرة على التمييز بين المرضى الذين يعانون من نظام التشغيل النقيلي
كما هو مبين في الشكل 11A، لم تلاحظ أي حالات ورم خبيث في المجموعة منخفضة المخاطر (TARGET، 90.25٪ وGSE21257، 58.34٪) مقارنة بالمجموعة عالية الخطورة (TARGET، 58.54٪ وGSE21257، 17.25٪). أيضًا، بالمقارنة مع المجموعة النقيلية، كانت درجة المخاطر أقل في المجموعة غير النقيلية (ص<0.01، الشكل 11ب،ج). أيضًا، أظهرت نتائج تحليل ROC أن الأداء التشخيصي للنموذج التنبؤي للتنبؤ بالانتشار النقيلي كان 0.659 و0.705 لـ TARGET وGSE21257، على التوالي (الشكل 11D، E). تظهر هذه النتائج أن نموذج المخاطر قد يتنبأ بالورم الخبيث لدى مرضى OS.
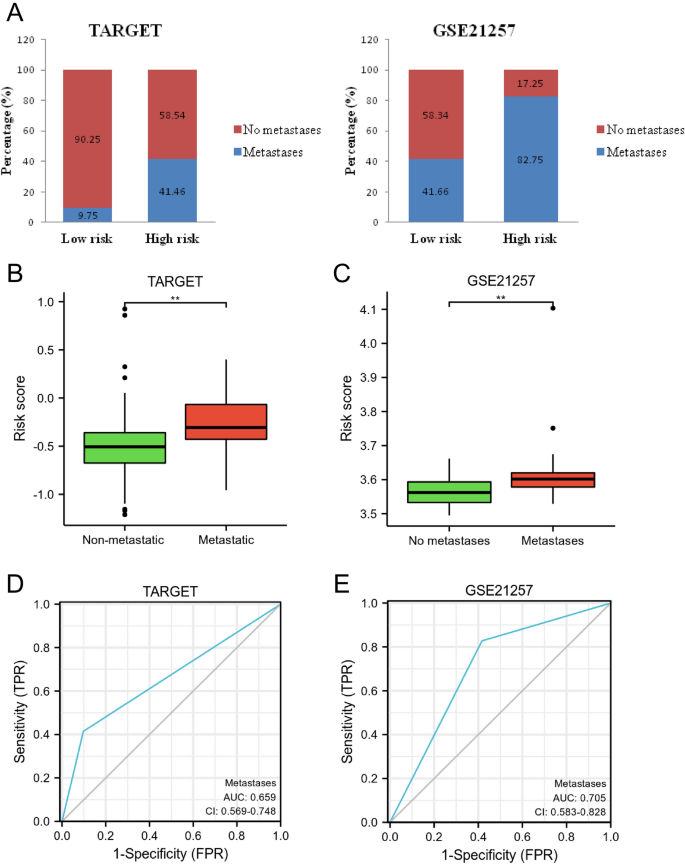
تقييم قدرة النموذج النذير على التنبؤ بالورم الخبيث لدى مرضى OS. (أ) مقارنات بين ورم خبيث وحالات ورم خبيث في المجموعات المنخفضة والعالية المخاطر. (ب) مقارنة درجات المخاطر في المجموعات النقيلية وغير النقيلية. (ج) تحليل ROC للأداء التشخيصي في التنبؤ بالانبثاث في نظام التشغيل.

“محبي البيرة. عالم موسيقى. متعصب للإنترنت. متواصل. لاعب. خبير طعام نموذجي. خبير قهوة.”






More Stories
تقدم بانيراي أربعة إصدارات مميزة لعلامة “Luna Rosa”.
تطرح Google تعزيزًا جديدًا للذكاء الاصطناعي لملايين هواتف Android القديمة
يوفر iOS 18 5 ميزات رائعة